유전자 돌연변이에 따른 주파수별 잔존청력 진행 패턴 고려해 인공와우 수술 시기 결정해야
분당서울대병원 이비인후과 최병윤 교수 연구팀(교신저자 최병윤 교수, 제1저자 이상연 전문의)은 다수의 연구결과를 통해 영상과 유전자에 기반을 둔 정밀의료적 인공와우 수술 기법을 세계 최초로 정립해 주목받고 있다.
이번 발표된 연구 결과들은 저명한 국제학술지 네이처의 자매지인 ‘사이언티픽 리포트(Scientific Reports)’와 이과학 분야 최고 학술지인 ‘이어 앤 히어링(Ear and Hearing)’에 각각 게재됐다.
18일 분당서울대병원에 따르면 정밀의료란 유전정보, 생활습관 등 개인의 건강정보를 바탕으로 하여 개인 맞춤 진단 및 치료 계획을 제공하는 것으로, 최근 많이 상용화 된 인공와우 수술에 있어서도 정밀의학적 치료방향을 찾는 것이 중요하다.
최 교수는 ‘전극 삽입 시 달팽이관의 손상을 최소화함과 동시에 신경원 세포를 가장 효율적으로 자극시키는 얇은 전극(slim modiolar electrodes)’을 이용한 인공와우 수술을 지난 2018년부터 시작해 약 300여 건 시행해오고 있다. 이는 국내 최다 경험이자 아시아에서도 가장 많은 경험을 보유한 수치다.
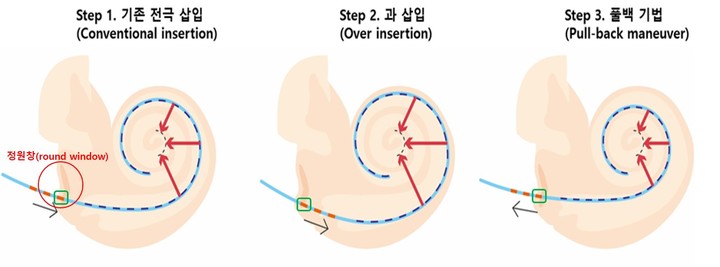
이 전극을 이용한 인공와우 수술 시 전극과 신경원 세포 사이의 거리는 수술 결과를 결정하는데 매우 중요한 요소로 작용한다. 최 교수는 이 전극을 가장 효율적으로 사용하기 위해 ‘풀백 수술 기법’을 국내에서 유일하게 적용하고 있는데, 이 기법은 전극의 위치를 재 교정하여 전극과 신경원 세포의 접근성을 극대화하는 방법이다.
현재까지 이 수술 기법을 통해 수술 받은 환자들에서 전극(전선)의 꼬임이나 전극 전위는 나타나지 않았고, 잔존 청력 또한 잘 유지시키는 것으로 확인돼 그 우수성을 인정받고 있다.
연구팀은 지난 2018년부터 2019년까지 분당서울대병원에서 이 수술 기법을 통해 인공와우 이식 수술을 받은 환자 38명(소아 난청 19명, 성인 난청 19명)을 분석했다. 분석 결과, 달팽이관의 크기가 작을수록 동일한 수술 기법 사용 시 전극 삽입 후 전극과 신경원 세포 사이의 간격이 멀어짐을 확인했고, 따라서 개인별 달팽이관의 크기를 고려해 전극삽입 깊이를 조절해야 한다는 사실을 도출했다.
더불어 연구팀은 전극과 신경원 세포 사이의 거리를 한눈에 확인할 수 있는 새로운 영상 평가 지표를 개발해, 수술 시 전극과 신경원 세포 사이의 거리를 실시간으로 확인하며 접근성을 최대화 할 수 있게 됐다.
뿐만 아니라 최 교수 연구팀은 유전자 돌연변이에 따른 난청 진행 양상의 차이점을 분석한 연구를 통해 보다 정밀의학적인 인공와우 수술법의 근거를 제시했다.
소아 난청의 가장 흔한 원인인 SLC26A4 유전자(에바스 기형의 원인 유전자)(22명)와 GJB2유전자(8명) 돌연변이에 의한 난청 환자를 비교 분석한 이 연구는 세계 최초로 유전자 돌연변이에 의한 난청 진행 양상의 차이점을 수치화했다는 점에서 의미가 있다.
수술 전 저음역에서 잔존 청력이 유지된 소아 환자들을 대상으로 평균 3년 이상 청력검사를 통해 경과를 관찰한 결과, SLC26A4 유전자 돌연변이에 의한 난청의 진행 속도는 1년 평균 10dB 이상 진행된 반면, GJB2 유전자는 1년 평균 5dB 진행돼 유전자에 따라 난청의 진행 속도가 상이한 것을 확인했다.
또한, 대표적 유전자 돌연변이라 할 수 있는 이 두 유전형에 따른 난청 진행 속도를 저·중·고주파수 별로 수치화하여, 향후 인공와우 수술 시기를 결정하는데 있어 중요한 지표로 활용될 수 있는 근거를 마련했다.
최병윤 교수는 이러한 연구결과를 바탕으로 “수술 전 영상검사와 유전자 분석을 통해 철저한 개인 맞춤별 인공와우 치료를 시행하고 있는 만큼, 적기에 치료를 받으면 치료 효과를 극대화할 수 있다”고 강조했다.
이어 최 교수는 “난청은 최대한 청각을 보존하는 방법으로 치료하게 되는데, 청력을 최대한 보존하려면 적극적으로 검사해 본인의 달팽이관 크기는 어떠한지, 난청 유전자 유무는 어떠한지 등을 정확히 파악하고 치료시기를 앞당겨야 한다”고 덧붙였다.


